Stem weevils and budworms: monitoring and control on 2 fronts - Cloned
At the end of a record number of rainy days, the clear skies and sudden, exceptional rises in temperature at the end of February were conducive to the drying out of the best-filtered plots and the advancement of the rapeseed stage, but also to major flights of stem weevils and leaf beetles. While current priorities are focused on nitrogen inputs at the end of winter, we must not neglect to monitor and control these two insects, which this year appear at the same time.
Rapeseed stem weevils can cause stem bursts, which penalize yield components, particularly in dry years. Egg-laying disrupts sap flow, making plants sensitive to subsequent stresses and limiting their ability to compensate. Hydric stress or an attack by another pest in spring on an oilseed rape previously weakened by stem weevil are thus more damaging. Control methods are still effective, but the positioning of the intervention is crucial to guarantee the effectiveness of the protection.
Peak of flights possibly reached at the end of February, on rapeseed at sensitivity stage
Southwest
As the weather warmed up at the beginning of the month, the first flights of stem weevils, mainly on cabbage but also on rapeseed, took place in the Occitanie and ex-Aquitaine regions, but at generally low levels on rapeseed crops still in vegetation recovery or early bolting. The drop in temperatures and return of rain over the following days were unfavorable to the intensification of flights and egg-laying activity by females.
The return of clear skies and exceptional temperatures over the last few days have been favorable to significant weevil flights, with the probability of captures and presence in plots currently reaching its peak, on oilseed rape crops in full bolting, mostly at D1-D2 stages (source: BSV Occitanie-Nouvelle Aquitaine), and for some weakened by excess winter water and lack of nitrogen when vegetation resumes.
As a general rule, it is advisableto intervene 8 - 10 days after the first "significant" captures, or ideally at the regional flight peak (consult the BSV for the date of the flight peak at regional level). In fact, the mere presence of the pest in the crop constitutes a nuisance threshold. The aim is to intervene when as many insects as possible are in the plot, and before egg-laying begins.
With the flight peak probably underway, an intervention could be launched in the week of March 02 to 09 to effectively control stem weevil populations, subject to a drop in catches within the BSV network next week.
Insecticide solutions still effective
The success of chemical control depends on the positioning of the intervention and the persistence of action. To date, Terres Inovia has not observed any decline in efficacy in the field. Monitoring results show no worrying emergence of resistance.
DECIS PROTECH 0.33 L/ha and KARATE ZEON 0.075 L/ha are effective in reducing rapeseed stem weevil damage (reduction in the number of deformed and/or shattered stems).
TREBON 30 EC is comparable to these references. In the case of late infestation and presence of budworms, it is also effective against the latter.
SHERPA 100 EW and CYTHRINE MAX are slightly behind. MAVRIK SMART, on the other hand, is inferior to the references on stem weevil and should be reserved for possible control of meligethes between stages D1 and E-F1.
Caution: TREBON 30 EC and MAVRIK SMART should be reserved for possible control of meligethes between stages D1 and E-F1.
Meligèthes: Vigilance is essential
A sudden and massive arrival
The exceptionally warm weather and sunny spells of the past few days have been very favorable to insect flights, including the meligèthe, which can easily be caught in tanks or observed in plots, particularly on the most advanced rapeseed plants. The beetle is above all a pollinator. Its diet is based on pollen. However, when flowers are still at bud stage, they perforate them to reach the stamens, which can damage the pistil and lead to abortion. The risk of losses is all the greater when the buds are small; but as soon as the flowers are open, the pollen is free to access, and the nuisance generally becomes nil and treatment unnecessary. Females lay eggs in the buds during flowering, but this does not damage the plant.
Visit your plots to assess the condition of your colza and the presence of the beetle
The more vigorous and healthy the crop, the more it can withstand the presence of budworms, even if they are abundant. On the contrary, the more stunted, stressed or constrained the crop, the more susceptible it will be to attack. Observing the condition of the rapeseed is therefore just as important as observing the pest.
Here are a few rules to bear in mind when characterizing the risk of meligèthes on rapeseed:
- Rapeseed fertilization: what to do if the soil is too wet Observe plots from the D1 stage (BBCH50), corresponding to the appearance of clustered buds still hidden under the leaves, to the F1 stage (BBCH60), corresponding to the first flowers opening on half the plants. At the D1 stage, when flower buds are present and still hidden under the terminal leaves, beetles are more difficult to observe. You need to take the time to analyze the area of leaves surrounding the buds. At stage D2 (BBCH53) and E (BBCH57), the buds are fully visible and the larches are easier to spot.
- Counting at the edges or on the tallest plants is not representative of the situation. It is advisable to count on 4 x 5 or 2 x 10 consecutive plants; then calculate an average or a % per plant to be compared with the thresholds mentioned in the table below, taking into account the crop's ability to compensate.
- Avoid trap plants if present.
- Vigilance must now be maintained through regular plant counts, in order to determine where you stand in relation to the thresholds.
- Vigilance is also essential in situations where a tall, very early variety (e.g. ES Alicia or DK Exavance) is mixed. This practice enables us to control certain weak to moderate attacks, but does not rule out monitoring! In the event of heavy attacks, beyond the thresholds indicated below on the plants of interest, control of the populations of meligèthes may be justified.
Control strategy: maintain the population at a tolerable level using appropriate specialties
The aim of the control strategy is to maintain the population at a tolerable level (and not to eradicate it), so that flowering can start without major delays, and so that compensation can be expressed to the full. Rapeseed has considerable capacity for compensation. When the crop is vigorous, it can withstand even heavy attacks by beetles.
Meligethes are resistant to "-ine" pyrethroids (lambda-cyhalothrin, deltamethrin, cypermethrin, etc.). Tau-fluvalinate and etofenprox are 2 pyrethroids that escape rapid metabolism by meligethes and retain their potential efficacy.
Active substances effective on meliger beetles :
- Etofenprox (TREBON,30EC, UPPERCUT 0.2 l/ha)
- Tau-fluvalinate (MAVRIK SMART, TALITA 0.2 l/ha)
In case of concomitant presence of meligethes and rapeseed stem weevils at the intervention threshold, give preference to the use of Etofenprox-based solutions, taking care to respect the conditions of use of the corresponding insecticide specialties.
Recommendations for use
Optimum spray volume of around 200 l/ha: to optimize the effectiveness of insecticide spraying, it is advisable to work at "normal" volumes, avoiding low volumes of less than 100 l/ha.
The context in which spraying is carried out is important: sprayer settings, climatic conditions, characteristics of the product applied.
Protection of bees: Dangerous for bees (phrase SPE8): to protect bees and other pollinating insects, do not apply during flowering and/or exudate production periods, with the exception of uses benefiting from the F, PE, or FPE bee label. In the event of late application (e.g. E stage with first flowers appearing), it is imperative to use effective solutions which benefit from a bee exemption: MAVRIK SMART, TREBON 30EC (use-by stage BBCH61). Please note: these applications are subject to a decree governing application times: 2 hours before sunset and 3 hours after sunset.
Reasonable use of these solutions is essential. Read labels and available documentation carefully, and follow recommendations for use.
Your regional contacts
- Alexandra DENOYELLE (a.denoyelle@terresinovia.fr) - Regional Development Engineer - Auvergne Rhône-Alpes and Provence Alpes Côte d'Azur
- Quentin LAMBERT (q.lambert@terresinovia.fr) - Regional Development Engineer - Occitanie
- Quentin LEVEL (q.level@terresinovia.fr) - Regional Development Engineer - Ex-Aquitaine, Gers, Hautes-Pyrénées

Stem weevils and budworms: monitoring and control on 2 fronts
At the end of a record number of rainy days, the clear skies and sudden, exceptional rises in temperature at the end of February were conducive to the drying out of the best-filtered plots and the advancement of the rapeseed stage, but also to major flights of stem weevils and leaf beetles. While current priorities are focused on nitrogen inputs at the end of winter, we must not neglect to monitor and control these two insects, which this year appear at the same time.
Rapeseed stem weevils can cause stem bursts, which penalize yield components, particularly in dry years. Egg-laying disrupts sap flow, making plants sensitive to subsequent stresses and limiting their ability to compensate. Hydric stress or an attack by another pest in spring on an oilseed rape previously weakened by stem weevil are thus more damaging. Control methods are still effective, but the positioning of the intervention is crucial to guarantee the effectiveness of the protection.
Peak of flights possibly reached at the end of February, on rapeseed at sensitivity stage
Southwest
As the weather warmed up at the beginning of the month, the first flights of stem weevils, mainly on cabbage but also on rapeseed, took place in the Occitanie and ex-Aquitaine regions, but at generally low levels on rapeseed crops still in vegetation recovery or early bolting. The drop in temperatures and return of rain over the following days were unfavorable to the intensification of flights and egg-laying activity by females.
The return of clear skies and exceptional temperatures over the last few days have been favorable to significant weevil flights, with the probability of captures and presence in plots currently reaching its peak, on oilseed rape crops in full bolting, mostly at D1-D2 stages (source: BSV Occitanie-Nouvelle Aquitaine), and for some weakened by excess winter water and lack of nitrogen when vegetation resumes.
As a general rule, it is advisableto intervene 8 - 10 days after the first "significant" captures, or ideally at the regional flight peak (consult the BSV for the date of the flight peak at regional level). In fact, the mere presence of the pest in the crop constitutes a nuisance threshold. The aim is to intervene when as many insects as possible are in the plot, and before egg-laying begins.
With the flight peak probably underway, an intervention could be launched in the week of March 02 to 09 to effectively control stem weevil populations, subject to a drop in catches within the BSV network next week.
Insecticide solutions still effective
The success of chemical control depends on the positioning of the intervention and the persistence of action. To date, Terres Inovia has not observed any decline in efficacy in the field. Monitoring results show no worrying emergence of resistance.
DECIS PROTECH 0.33 L/ha and KARATE ZEON 0.075 L/ha are effective in reducing rapeseed stem weevil damage (reduction in the number of deformed and/or shattered stems).
TREBON 30 EC is comparable to these references. In the case of late infestation and presence of budworms, it is also effective against the latter.
SHERPA 100 EW and CYTHRINE MAX are slightly behind. MAVRIK SMART, on the other hand, is inferior to the references on stem weevil and should be reserved for possible control of meligethes between stages D1 and E-F1.
Caution: TREBON 30 EC and MAVRIK SMART should be reserved for possible control of meligethes between stages D1 and E-F1.
Meligèthes: Vigilance is essential
A sudden and massive arrival
The exceptionally warm weather and sunny spells of the past few days have been very favorable to insect flights, including the meligèthe, which can easily be caught in tanks or observed in plots, particularly on the most advanced rapeseed plants. The beetle is above all a pollinator. Its diet is based on pollen. However, when flowers are still at bud stage, they perforate them to reach the stamens, which can damage the pistil and lead to abortion. The risk of losses is all the greater when the buds are small; but as soon as the flowers are open, the pollen is free to access, and the nuisance generally becomes nil and treatment unnecessary. Females lay eggs in the buds during flowering, but this does not damage the plant.
Visit your plots to assess the condition of your colza and the presence of the beetle
The more vigorous and healthy the crop, the more it can withstand the presence of budworms, even if they are abundant. On the contrary, the more stunted, stressed or constrained the crop, the more susceptible it will be to attack. Observing the condition of the rapeseed is therefore just as important as observing the pest.
Here are a few rules to bear in mind when characterizing the risk of meligèthes on rapeseed:
- Rapeseed fertilization: what to do if the soil is too wet Observe plots from the D1 stage (BBCH50), corresponding to the appearance of clustered buds still hidden under the leaves, to the F1 stage (BBCH60), corresponding to the first flowers opening on half the plants. At the D1 stage, when flower buds are present and still hidden under the terminal leaves, beetles are more difficult to observe. You need to take the time to analyze the area of leaves surrounding the buds. At stage D2 (BBCH53) and E (BBCH57), the buds are fully visible and the larches are easier to spot.
- Counting at the edges or on the tallest plants is not representative of the situation. It is advisable to count on 4 x 5 or 2 x 10 consecutive plants; then calculate an average or a % per plant to be compared with the thresholds mentioned in the table below, taking into account the crop's ability to compensate.
- Avoid trap plants if present.
- Vigilance must now be maintained through regular plant counts, in order to determine where you stand in relation to the thresholds.
- Vigilance is also essential in situations where a tall, very early variety (e.g. ES Alicia or DK Exavance) is mixed. This practice enables us to control certain weak to moderate attacks, but does not rule out monitoring! In the event of heavy attacks, beyond the thresholds indicated below on the plants of interest, control of the populations of meligèthes may be justified.
Control strategy: maintain the population at a tolerable level using appropriate specialties
The aim of the control strategy is to maintain the population at a tolerable level (and not to eradicate it), so that flowering can start without major delays, and so that compensation can be expressed to the full. Rapeseed has considerable capacity for compensation. When the crop is vigorous, it can withstand even heavy attacks by beetles.
Meligethes are resistant to "-ine" pyrethroids (lambda-cyhalothrin, deltamethrin, cypermethrin, etc.). Tau-fluvalinate and etofenprox are 2 pyrethroids that escape rapid metabolism by meligethes and retain their potential efficacy.
Active substances effective on meliger beetles :
- Etofenprox (TREBON,30EC, UPPERCUT 0.2 l/ha)
- Tau-fluvalinate (MAVRIK SMART, TALITA 0.2 l/ha)
In case of concomitant presence of meligethes and rapeseed stem weevils at the intervention threshold, give preference to the use of Etofenprox-based solutions, taking care to respect the conditions of use of the corresponding insecticide specialties.
Recommendations for use
Optimum spray volume of around 200 l/ha: to optimize the effectiveness of insecticide spraying, it is advisable to work at "normal" volumes, avoiding low volumes of less than 100 l/ha.
The context in which spraying is carried out is important: sprayer settings, climatic conditions, characteristics of the product applied.
Protection of bees: Dangerous for bees (phrase SPE8): to protect bees and other pollinating insects, do not apply during flowering and/or exudate production periods, with the exception of uses benefiting from the F, PE, or FPE bee label. In the event of late application (e.g. E stage with first flowers appearing), it is imperative to use effective solutions which benefit from a bee exemption: MAVRIK SMART, TREBON 30EC (use-by stage BBCH61). Please note: these applications are subject to a decree governing application times: 2 hours before sunset and 3 hours after sunset.
Reasonable use of these solutions is essential. Read labels and available documentation carefully, and follow recommendations for use.
Your regional contacts
- Alexandra DENOYELLE (a.denoyelle@terresinovia.fr) - Regional Development Engineer - Auvergne Rhône-Alpes and Provence Alpes Côte d'Azur
- Quentin LAMBERT (q.lambert@terresinovia.fr) - Regional Development Engineer - Occitanie
- Quentin LEVEL (q.level@terresinovia.fr) - Regional Development Engineer - Ex-Aquitaine, Gers, Hautes-Pyrénées

All you need to know about sunflower phomopsis
Sunflower phomopsis is a disease caused by a necrotrophic ascomycete fungus belonging to the Diaporthe genus.
Agent pathogène et hôte
Le phomopsis du tournesol est une maladie causée par un champignon ascomycète nécrotrophe appartenant au genre Diaporthe. Cet agent pathogène se présente sous deux formes biologiques : une forme sexuée, appelée Diaporthe helianthi, et une forme asexuée, Phomopsis helianthi. Cette espèce est historiquement la plus couramment impliquée dans les attaques observées sur tournesol. Toutefois, des travaux plus récents ont mis en évidence l’existence d’autres espèces du genre Diaporthe capables d’infecter cette culture, notamment D. gulyae, D. kongii, D. masirevicii et D. novem.
Phomopsis helianthi a été décrit pour la première fois à la fin des années 1970 dans l’ex-Yougoslavie à la suite d’épidémies sévères sur tournesol. En France, la maladie est identifiée pour la première fois en 1984 dans une zone située entre Toulouse et Carcassonne. À partir du milieu des années 1990, le phomopsis s’est progressivement étendu à l’ensemble des régions de culture du tournesol. Aujourd’hui, cette maladie est responsable de pertes de rendement importantes dans plusieurs pays producteurs, notamment en Europe de l’Est, en Russie, aux États-Unis et en Australie.
L’hôte principal de la maladie est le tournesol cultivé (Helianthus annuus). D’autres espèces d’Astéracées telles que Arctium lappa, Xanthium italicum ou Xanthium strumarium ont été signalées comme hôtes potentiels, mais leur rôle dans pour la survie et la propagation du phomopsis n’a pas été clairement démontré.
Symptômes
Les premiers symptômes du phomopsis apparaissent généralement après la floraison, bien que les contaminations puissent avoir lieu plus précocement. Ils se manifestent initialement sur les feuilles, sous la forme de taches triangulaires brunâtres, souvent bordées d’un halo chlorotique jaune, localisées en bordure du limbe. Ces taches s’étendent progressivement le long des nervures principales en direction du pétiole, ce qui constitue un élément caractéristique de la maladie.
À un stade plus avancé, les feuilles atteintes se flétrissent puis se dessèchent. Le champignon progresse de manière systémique le long du pétiole pour atteindre la tige. Cette phase de colonisation est lente et souvent asymptomatique pendant plusieurs semaines, ce qui explique le décalage fréquent entre la date de contamination et la date d’apparition sur tige.
Les lésions observées sur tige sont allongées, de couleur brun foncé à brun grisâtre, et sont le plus souvent localisées au niveau des nœuds, à l’insertion des pétioles. Elles peuvent atteindre une longueur de 15 à 20 cm et évoluer jusqu’à encercler complètement la tige. Dans ce cas, la circulation de la sève est interrompue, ce qui entraîne un dessèchement prématuré du capitule ainsi qu’une fragilisation importante de la tige, susceptible de casser sous l’effet du vent, de la pluie ou lors de la récolte.
Des symptômes peuvent également être observés sur le capitule. Ils se traduisent par l’apparition de petites taches brunes à l’insertion des bractées ou des folioles situées à l’arrière du capitule, puis par une extension progressive vers la tige. Dans les situations les plus sévères, l’ensemble du capitule peut se dessécher prématurément.
Attention aux confusions !
Les symptômes du phomopsis peuvent être confondus avec ceux d’autres maladies du tournesol.
- Sur feuilles, une confusion est possible avec le verticillium, mais la nécrose du phomopsis suit les nervures du limbe foliaire, contrairement à celle du verticillium, qui est inter-nervaire.
- Sur tige, le phomopsis peut être confondu avec le phoma ; toutefois il se caractérise par des taches plus foncées, souvent noires, sans provoquer de casse de tige.
Importance de la maladie
En France, le phomopsis du tournesol était très fréquent jusqu’à la fin des années 1990. Depuis le milieu des années 2010, sa fréquence a nettement diminué, jusqu’à devenir presque absente certaines années, à l’exception de quelques campagnes ponctuelles, comme en 2021, où des signalements ont été observés.
Malgré cette évolution, la maladie reste à surveiller dans certaines régions, notamment dans Centre et Centre-Est, où elle est historiquement la plus fréquemment observée.
La nuisibilité du phomopsis peut être importante. En conditions favorables, les pertes de rendement peuvent atteindre jusqu’à 40 %, auxquelles s’ajoute une baisse de la teneur en huile des graines pouvant atteindre 25 %. Il est généralement admis qu’un taux de 10 % de tiges présentant des lésions encerclantes peut entraîner une perte de rendement comprise entre 1 et 3 quintaux par hectare, ainsi qu’une diminution d’environ un point de teneur en huile. La maladie est surtout nuisible dans le Nord-Est.
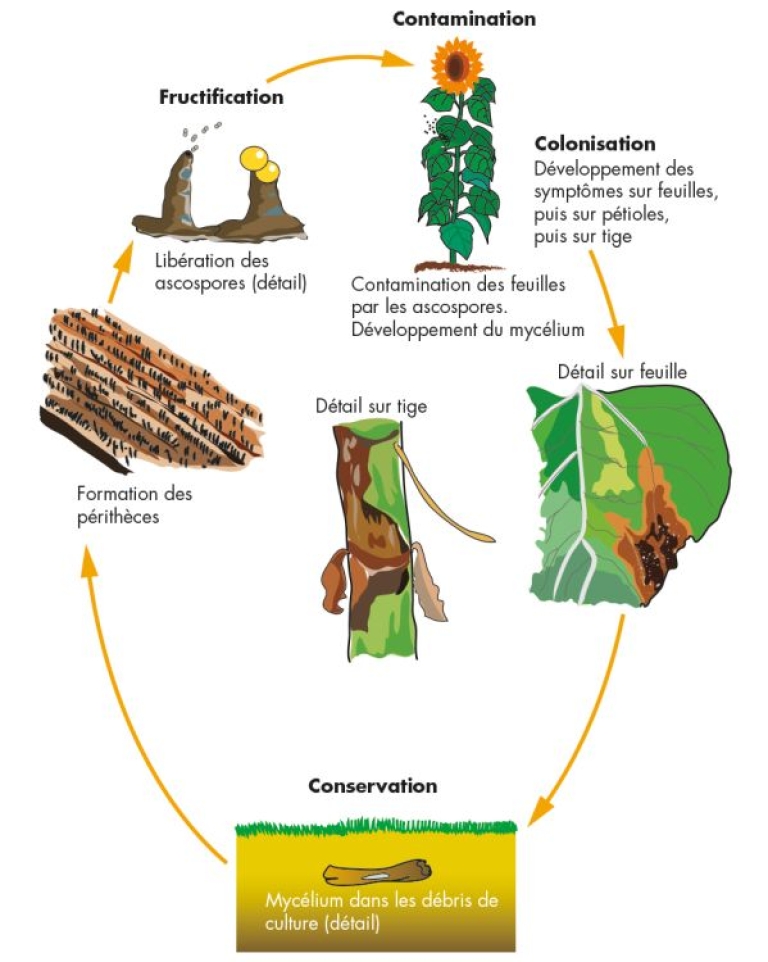
Cycle de vie
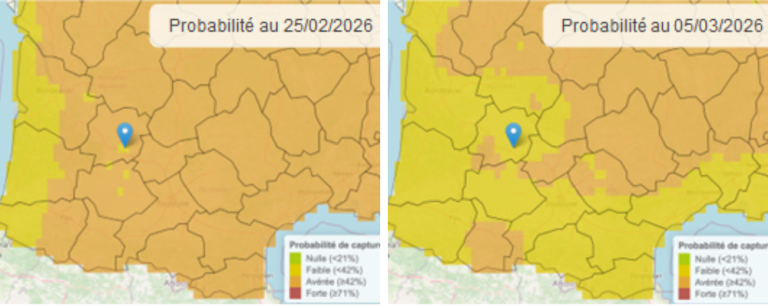
Le champignon hiverne sous forme de mycélium et de périthèces sur les résidus de culture de tournesol présents à la surface du sol. À la fin de l’hiver, lorsque les températures atteignent environ 10 °C, les périthèces se forment. En conditions d’humidité suffisante, ils libèrent des ascospores, qui constituent l’inoculum primaire, qui pourront être émises de façon progressive avec des pics au moments des épisodes pluvieux. Ces spores sont disséminées par le vent ainsi que par les éclaboussures de pluie et contaminent les feuilles du tournesol.
Après l’infection des feuilles, le mycélium colonise les espaces intercellulaires, progresse le long des nervures et de la nervure centrale, puis migre vers le pétiole. Il atteint ensuite la tige de manière systémique, où se développe une lésion nécrotique allongée. Les pertes de rendement apparaissent lorsque les tissus conducteurs de la tige sont envahis et que le système vasculaire est obstrué. La plante se flétrit alors progressivement et la tige, fragilisée, peut casser sous le poids du capitule ou à la suite d’un choc.
Des infections secondaires peuvent être observées à partir de conidies produites dans les lésions de tige. Toutefois, ces conidies semblent avoir un rôle limité dans le développement de l’épidémie. L’agent pathogène est capable de survivre jusqu’à cinq ans sur les résidus de culture, en fonction des pratiques agronomiques et des conditions météorologiques.
Facteurs favorables
Le développement du phomopsis est étroitement dépendant des conditions climatiques. Des températures comprises entre 20 et 24 °C, associées à une humidité relative supérieure à 90 % pendant une durée prolongée, constituent des conditions particulièrement favorables à l’infection et à la progression du champignon.
Certaines pratiques agronomiques peuvent également favoriser l’apparition de la maladie.
Un semis précoce augmente le risque d’attaque sévère, car il favorise la coïncidence entre la période de sensibilité maximale du tournesol, située autour du stade bouton floral, et les périodes climatiques favorables aux contaminations.
Une densité de peuplement élevée entraîne une mauvaise circulation de l’air au sein du couvert végétal et favorise le maintien d’une forte humidité, condition indispensable au développement du phomopsis. Enfin, une fertilisation azotée excessive ainsi qu’une irrigation autour de la floraison peuvent accentuer la gravité des attaques.
Diversité de l’agent pathogène
La diversité des agents responsables du phomopsis varie selon les régions du monde. En France et plus largement en Europe, Diaporthe helianthi est l’espèce majoritairement retrouvée. En Australie, les épidémies sont principalement dues à Diaporthe gulyae, tandis qu’aux États-Unis, ces deux espèces coexistent.
La diversité intra-spécifique de Phomopsis helianthi reste encore peu documentée. À ce jour, il n’existe pas de dispositif de surveillance des populations en France. Toutefois, certaines études ont mis en évidence des différences d’agressivité entre isolats, suggérant une variabilité au sein des populations de cet agent pathogène.
Leviers de lutte
La gestion durable du phomopsis repose sur une approche intégrée, combinant plusieurs leviers complémentaires, à raisonner à l’échelle de la parcelle, de la rotation et du long terme.
Pratiques agronomiques
Les pratiques agronomiques jouent également un rôle majeur dans la réduction du risque :
- allonger la rotation du tournesol, idéalement avec un retour tous les cinq ans
L’allongement de la rotation du tournesol permet de réduire la quantité de résidus infectés disponibles et de limiter la pression d’inoculum d’une campagne à l’autre. Un retour trop fréquent du tournesol favorise au contraire l’accumulation de l’inoculum et augmente le risque d’infections précoces.
- broyer et enfouir les résidus de culture à plus de cinq centimètres de profondeur
Le broyage et l’enfouissement partiel des résidus contribuent à accélérer leur dégradation et à réduire la capacité du champignon à produire des périthèces viables.
- adapter les dates de semis
Un semis plus tardif peut provoquer la formation d’un couvert moins dense au moment des périodes à risque (périodes pluvieuses)
- éviter des densités de peuplement excessives
Une densité de peuplement élevée favorise la fermeture rapide du couvert, limite la circulation de l’air et augmente la durée pendant laquelle l’humidité relative reste élevée à l’intérieur de la végétation. Ces conditions sont particulièrement favorables aux infections foliaires, qui constituent la première étape du développement de la maladie
Résistances variétales
La tolérance variétale constitue un moyen de lutte efficace. Dans les zones à risque, opter pour des variétés très peu sensibles (TPS). Les variétés peu sensibles (PS) sont conseillées uniquement chez les producteurs prêts à traiter si nécessaire. Sur le reste du territoire, le choix variétal n’est pas contraint.
Lutte fongicide
La protection fongicide contre le phomopsis doit être considérée comme un levier d’appoint, dont l’efficacité dépend fortement du contexte. Les traitements visent essentiellement à limiter les infections foliaires précoces, afin de réduire la probabilité de progression du champignon vers la tige. Le recours à cette protection fongicide doit être raisonné en tenant compte du risque régional, de la sensibilité variétale, des caractéristiques de la parcelle et des informations issues des Bulletins de Santé du Végétal. Consultez le guide de culture tournesol Terres Inovia pour les recommandations de traitements.
Tout savoir sur le mildiou du tournesol
Plasmopara halstedii, agent responsable du mildiou du tournesol, est un oomycète biotrophe obligatoire, spécialiste, capable de se conserver pendant 10 ans dans le sol.
Agent pathogène et hôte
Plasmopara halstedii, agent responsable du mildiou du tournesol, est un oomycète biotrophe obligatoire, spécialiste, capable de se conserver pendant 10 ans dans le sol. Le mildiou est capable d’attaquer plusieurs Astéracées dont les espèces Hfelianthus comme H. argophyllus, H. debilis et H. petiolaris, et aussi la forme sauvage et cultivée de H.annuus, le tournesol. Plasmopara halstedii peut également attaquer d’autres Asteraceae comme Bidens, Artemisia, Xanthium, qui pourraient être de potentiels réservoirs d’inoculum.
Comme le mildiou est un agent pathogène biotrophe obligatoire, sa survie en absence de tournesol repose sur des plantes relais. Les principales plantes relais (de P. halstedii vers le tournesol) à considérer sont Ambrosia artemisiifolia, Xanthium strumarium, Iva xanthiifolia et Senecio vulgaris, qui sont parfois abondantes dans les parcelles cultivées en tournesol. Du fait de leur proximité botanique avec H. annuus, ces espèces sont peu sensibles à la plupart des herbicides utilisés dans cette culture.
| Nom latin | Nom courant | Nom latin | Nom courant |
| Ageratum sp. | Agératum | Helianthus giganteus | Tournesol géant |
| Ageratum houstonianum | Agératum du Mexique | Helianthus grosseserratus | Hélanthe à grosses dents |
| Ambrosia artemisiifolia | Ambroisie à feuilles d’armoise | Helianthus hirsutus | Tournesol hérissé |
| Artemisia vulgaris | Armoise commune | Helianthus nuttallii | Tournesol de Nuttall |
| Centaurea sp. | Centaurée | Helianthus petiolaris | Tournesol à pétiole |
| Chrysanthemum sp. | Chrysanthème | Helianthus rigidus | Tournesol rigide |
| Cineraria sp. | Cinéraire | Helianthus scaberrimus | Tournesol rude |
| Clibadium sp. | Clibadie | Helianthus strumosus | Tournesol à rhizomes |
| Coreopsis sp. | Coréopsis | Helianthus subrhomboideus | Tournesol subrhombique |
| Coreopsis lanceolata | Coréopsis lancéolé | Helianthus tuberosus | Topinambour |
| Dimorphotheca sp. | Ostéospermum / Marguerite africaine | Helianthus occidentalis | Tournesol occidental |
| Elephantopus sp. | Éléphantope | Helianthus debilis | Tournesol délicat |
| Emilia sp. | Émilie | Helianthus lenticularis | Tournesol lenticulaire |
| Erigeron sp. | Vergerette | Iva sp. | Iva |
| Eupatorium sp. | Eupatoire | Petasites sp. | Pétasite |
| Eupatorium ageratoides | Eupatoire agératoïde | Rudbeckia sp. | Rudbeckie |
| Eupatorium purpureum | Eupatoire pourpre | Rudbeckia fulgida | Rudbeckie brillante |
| Eupatorium rugosum | Eupatoire rugueuse | Senecio sp. | Séneçon |
| Franseria sp. | Franseria | Venidium sp. | Venidium |
| Gerbera jamesonii | Gerbéra | Verbesina sp. | Verbesine |
| Helianthus sp. | Tournesol | Vernonia sp. | Vernonie |
| Helianthus annuus | Tournesol commun | Xanthium strumarium | Lampourde commune |
| Helianthus argophyllus | Tournesol argenté | Ximenesia sp. | Ximenesia |
| Helianthus divaricatus | Tournesol à feuilles écartées | Zinnia sp. | Zinnia |
Symptômes
Les symptômes provoqués par le mildiou sur le tournesol sont multiples. Selon le stade d’infection de la plante, les symptômes peuvent aller jusqu’à de la mort de la plantule, si l’attaque est très précoce.
En début de cycle, les plantules contaminées présentent un retard de croissance, elles apparaissent « rabougries », montrent des cotylédons jaunes. Des zones décolorées vert plus clair sont visibles sur les feuilles, dont la face inférieure est recouverte d’un feutrage blanc plus ou moins intense : ce feutrage correspond aux sporulations du mildiou, à partir desquelles pourront se déclarer des contaminations secondaires mais surtout « se fabriquer » l’inoculum pour les campagnes suivantes. Le mildiou va peu à peu coloniser tous les tissus de la plante et « monter dans les étages » : on dit qu’il est systémique et son développement à l’intérieur de la plante entraîne un nanisme caractéristique : les entre-nœuds sont raccourcis.
Les symptômes courants lors d’une attaque sont :
- Nanisme de la plante
- Port à plat du capitule
- Symptômes en « ailes de fougère »
- Présence de chlorose sur les feuilles délimitées par les nervures
- Blanchiment des feuilles
- Sporulation blanche visible d’abord sur la face inférieure des feuilles
- Capitule stérile
Une visite en début de campagne permet de faire le point sur l’état de santé « mildiou » de la parcelle. Cette visite précoce présente le grand avantage de ne pas passer à côté des symptômes de mildiou, qui peuvent être plus difficiles à repérer lorsque le couvert se développe et les plantes grandissent. Souvent, un petit foyer de mildiou se déclare à l’entrée de parcelle, là où le passage du matériel agricole a créé des zones de tassement favorables à l’accumulation d’eau libre. N’hésitez pas à rentrer plus avant dans la parcelle afin de compléter votre diagnostic !
Attention, ne pas confondre mildiou et rouille blanche
Des attaques précoces de rouille blanche peuvent parfois se manifester : celles-ci n’occasionnent pas de nanisme. Des cloques de couleur vert clair se développent sur les feuilles. Sur leur face inférieure, les sporulations du champignon forment des croûtes et non un feutrage homogène.
Cycle de vie
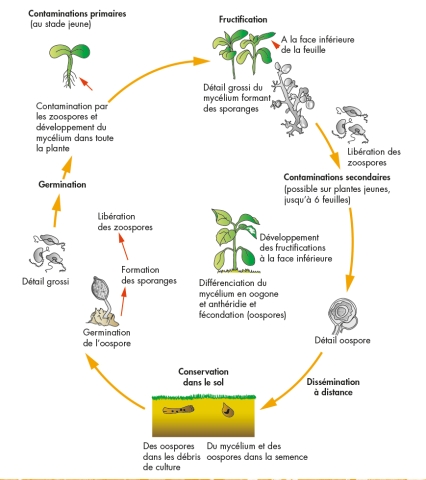
Bien que P. halstedii puisse être dispersé par le vent, l'eau et via les semences contaminées, il s'agit principalement d'un agent pathogène transmis par le sol. Au champ, les infections racinaires des jeunes plants de tournesol sont responsables des symptômes les plus graves et possèdent un fort impact sur le rendement.
Les zoospores de Plasmopara halstedii sont libérés soit à partir de sporanges oosporés (au printemps) soit à partir de sporanges asexués (du printemps à l'été) et peuvent infecter les jeunes plants de tournesol.
L’infection primaire se déroule au printemps et se passe sous forme souterraine via la germination d’oospores. Dans des conditions humides et fraîches, ces oospores vont entraîner la formation de zoosporanges, une structure de fructification produisant les zoospores. Ces zoospores sont biflagellées et vont aller infecter les racines de la plante. La contamination secondaire, contrairement à la primaire, se produit en phase aérienne. Les sporangiophores qui se trouvent sur les cotylédons ou sur la face inférieure des feuilles, vont entraîner la formation de sporanges qui seront disséminés par le vent, et produiront les zoospores responsables de l’infection secondaires. Cette étape est responsable des infections tardives des plantes voisines et contribue à la dissémination de l’agent pathogène.
Toute attaque même minime, contribue à alimenter le réservoir d’inoculum dans le sol.
Importance
Le mildiou est l’une des principales maladies affectant la production de tournesol. Cet agent pathogène a été observé pour la première fois en Amérique du Nord en 1888, puis en Russie et en Europe aux alentours de 1960. Cette introduction en Europe est probablement la conséquence d’une importation de graines contaminées. Depuis les années 1992 et jusqu’en 2019, ce pathogène a été soumis à un régime de quarantaine en Europe.
L’impact global de cette maladie sur le rendement a été estimé à 3,5% de la production de graine en Europe, avec l’utilisation des méthodes de contrôle couramment utilisées.
En général, les attaques de mildiou impactent peu le potentiel de production des parcelles de tournesol. Cependant, certains cas bien plus graves peuvent se manifester à l’occasion de conditions favorables (rotation, choix variétal, pluviométrie), plus le pourcentage de pieds nanifié dans la parcelle est important, plus la perte de rendement sera élevée. Dans le Sud-Ouest, les années 2019 et 2020 ont pu marquer les mémoires. En 2025, une situation inhabituelle a été constatée, des cas d’attaques sévères ont été observées dans le Nord-Est.
La nuisibilité des attaques primaires de mildiou est estimée à 1% de perte de rendement pour 1% de plantes nanifiées. Elle est donc significative en cas d’attaque généralisée ou par grands foyers mais quasi-nulle lorsque quelques pieds isolés sont touchés, ou qu’un petit foyer est présent à l’entrée de la parcelle.
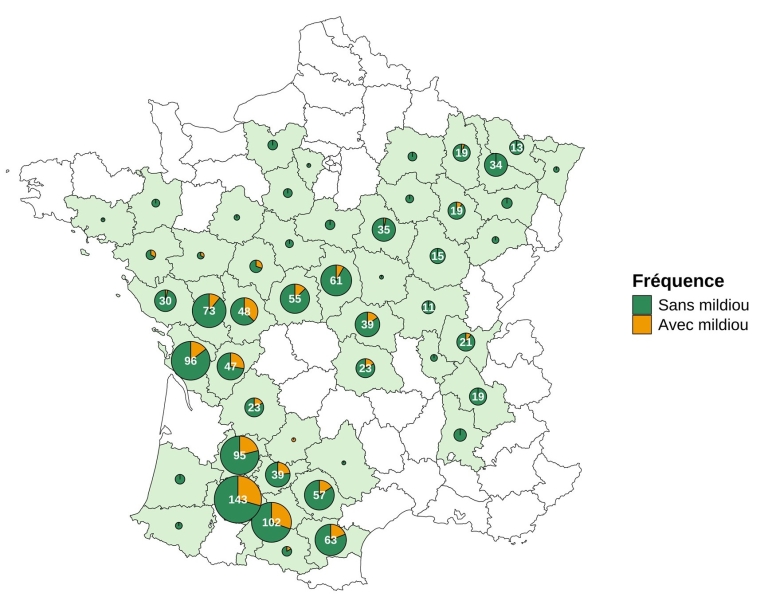
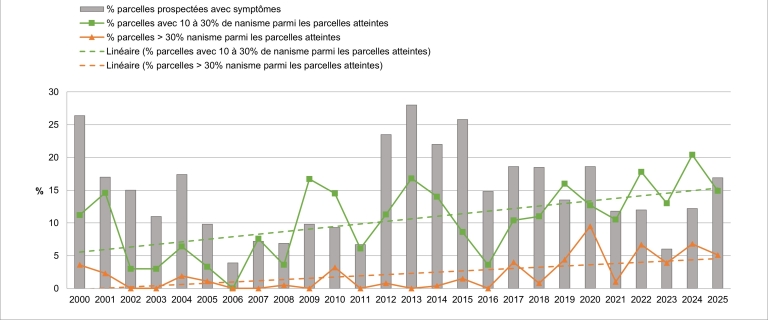
La surveillance du territoire national a mis en évidence une pression mildiou en augmentation depuis 6 ans : entre 12 et 19% de parcelles touchées, avec une augmentation significative de la proportion des attaques graves à plus de 10% de pieds nanifiés.
Facteurs favorables
Le retour trop fréquent du tournesol favorise le développement de la maladie. En effet les parcelles les plus attaquées sont celles ou le tournesol revient un an sur deux dans la rotation.
Le mildiou se développant lors de conditions très humides et fraîche, semer dans un sol mal ressuyé, froid et lorsque de fortes pluies sont annoncées sont des conditions favorables au développement de l’infection.
Le mauvais désherbage des parcelles de tournesol de toutes les espèces pouvant héberger le mildiou et les repousses de tournesol, favorise le développement de la maladie.
La culture de plantes hôtes du mildiou en interculture, tel que le niger ou encore la sylphie, est un autre facteur favorable au développement de la maladie.
Diversité de l’agent pathogène
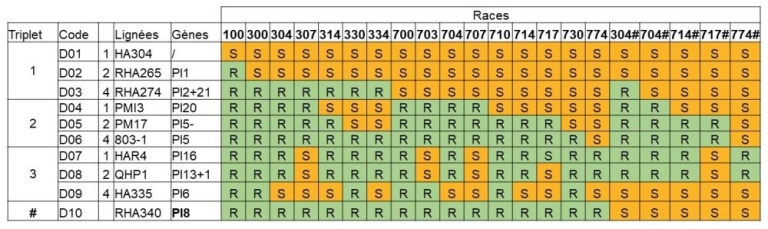
Les races de mildiou sont déterminées selon leur virulence vis-à-vis d’une gamme de lignées différentielles.
Tableau : lignées différentielles utilisées pour la détermination des races de mildiou en France. S : la race est virulente, R : la race est avirulente
Plasmopara halstedii est apparu en France pour la première fois en 1966 avec la race 100. Par la suite, la maladie fut éradiquée grâce à l’utilisation des résistances variétales. Néanmoins, la réapparition du mildiou en 1988 a tiré la sonnette d’alarme, et une surveillance annuelle a été mise en place en France en 1990. Cette surveillance nationale couvre l’ensemble des zones de production. En 1999, seulement deux races ont été détectées sur le territoire français, les races 703 et 710. Depuis le début des années 2000, les races dites « récentes » sont régulièrement détectées, il s’agit des race 304, 307, 314, 334, 704 et 714, en plus des races dites « anciennes », 100, 710 et 703 (CETIOM & INRAE, 2011). En France, depuis le début de la surveillance, environ 24 races ont été identifiées selon leur profil de virulence.
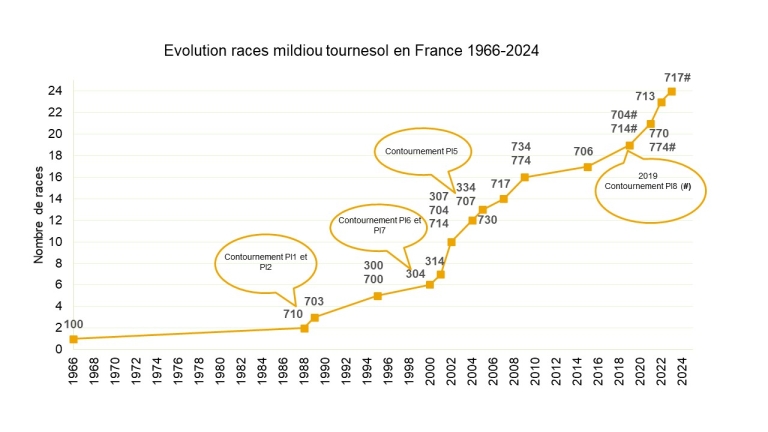
Graphique de l’évolution du nombre de races de mildiou du tournesol en France de 2000 à 2024.
Les races de mildiou en France sont en constante évolution. Au début des années 2000 et jusqu’en 2010, les anciennes races de mildiou 703 et 710 représentaient la majorité de la fréquence des races retrouvées en France, avec une fréquence de la race 710 souvent aux alentours des 70%. Par la suite, c’est la race 714, apparue pour la première fois en 2002, qui a dominé le paysage. En effet, contrairement aux races 703 et 710, la race 714 est virulente contre le gène de résistance Pl6. L’utilisation de plus en plus répandue de ce gène dans les variétés cultivées a entraîné une augmentation de fréquence de cette race dans le paysage.
La race 704 a également été retrouvée en fréquence élevée parallèlement à la race 714. Mais depuis les années 2019, de nouvelles races de mildiou sont apparues et dominent à présent le paysage, il s’agit des races 774#, 704# et plus particulièrement la race 714#. Ces races sont capables d’infecter les variétés comportant le gène de résistance Pl8 (#). Ce gène a été introduit à une fréquence significative depuis quelques années ce qui a entraîné l’apparition de races virulentes correspondantes.
Leviers de lutte
La gestion durable du mildiou passe par une protection intégrée où tous les leviers de lutte doivent être raisonnés à la parcelle, dans la rotation, et pour le long terme.
Pratiques agronomiques
La lutte contre le mildiou passe par des mesures agronomiques simples mais efficaces qui permettent de réduire le risque :
- Allonger les rotations de tournesol.
- Semer dans un sol bien ressuyé et réchauffé sans annonces de fortes pluies les jours suivant le semis.
- Détruire des parcelles cultivées en tournesol toutes les espèces pouvant héberger le mildiou.
- Eviter les plantes hôte en interculture.
Résistances variétales
Ces bonnes pratiques agronomiques peuvent se combiner au choix variétal pour favoriser la diminution du risque d’apparition de la maladie.
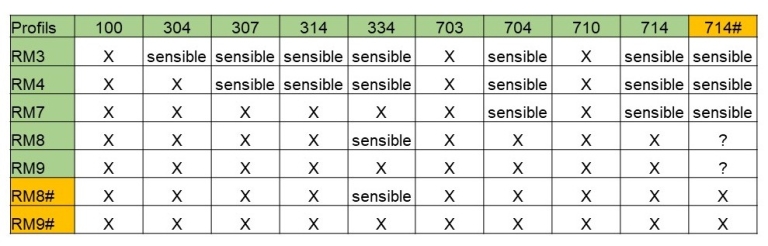
La résistance des variétés au mildiou est définie par leur profil RM. Il existe des variétés dites RM9, c’est-à-dire qu’elles sont résistantes aux 9 races officielles de mildiou : 100, 304, 307, 314, 334, 703, 704, 710 et 714, RM8, résistantes à 8 des 9 races (sensible à la race 334). Depuis quelques années, des profils de résistance #, RM8# et RM9#, sont apparus sur le marché, ces variétés sont résistantes à la race 714#, en plus des autres, race la plus communément retrouvée lors d’attaque de variétés RM9.
A ce jour il existe 88 variétés résistantes à la race majoritaire de mildiou (RM9#) en France, leur utilisation permet de lutter contre la maladie. L’alternance des variétés permet de changer, au fil des campagnes, les gènes de résistances auxquels on expose le mildiou dans la parcelle, et donc de réduire le contournement de ces résistances. En effet, cultiver des variétés possédant un même gène de résistance au fil des campagnes entraine une forte pression de sélection sur le mildiou, vis-à-vis de ce gène, ce qui favorise les cas de contournements.
Traitement de semence
Le recours au traitement de semence est possible mais non obligatoire. Son utilisation est à raisonnée en fonction de l’historique mildiou de la parcelle ainsi que de la variété utilisée. A ce jour, il existe deux spécialités à base d’oxathiapriproline (LUMISENA et PLENARIS), disponibles comme traitement de semence mildiou.
LUMISENA (n°2200078) de la société CORTEVA et PLENARIS (n°2200736) de la société SYNGENTA sont deux traitements de semences à base d’oxathiapiproline à 200 g/l en formulation FS.
Cette substance active connue notamment en vigne (ZORVEC) pour sa bonne action contre le mildiou de la vigne est un inhibiteur de la protéine de liaison à l’oxystérol. Elle intervient dans l’équilibre, le transport et le stockage des lipides de la cellule du champignon. L’oxathiapiproline est classé dans le groupe 49 du FRAC (Fongicide Résistance Action Committee) qui juge le risque de résistance comme moyen à élevé. C’est en effet un fongicide à mode d’action unisite. Il est déconseillé de l’employer seul. C’est un point commun à toutes les luttes durables : associer deux modes d’action efficace, que ce soit en mildiou vigne, fongicides céréales ou colza ou mildiou du tournesol.
Si disponible, Terres Inovia conseil d’associer l’oxathiapiproline à un autre anti-mildiou efficace afin de limiter la pression de sélection.
Attention, l’utilisation de semences traitées doit être réfléchi au cas par cas et ne doit pas être systématique, afin de ne pas favoriser l’apparition de résistances chez le mildiou
Le raisonnement pour la lutte contre le mildiou doit être tenu à la parcelle car il dépend de l’historique de chacune :
- la parcelle a-t-elle subi des attaques de mildiou sur les 5 dernières campagnes ?
- quelles variétés (génétique, profil RM) y ont été cultivées ?
- avec quel(s) traitement(s) de semences anti-mildiou ?
C’est sur ces questions que se base notre position technique.
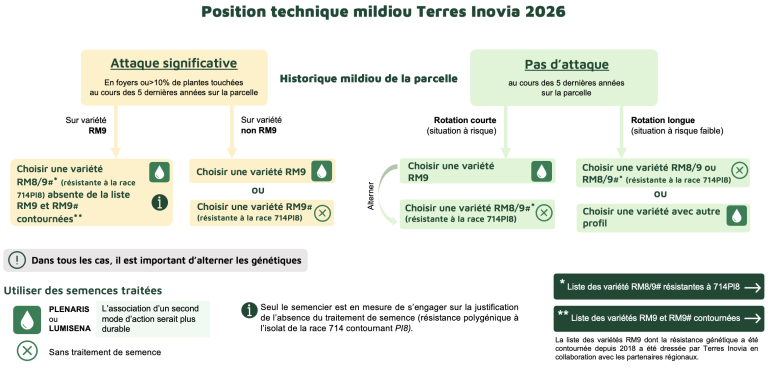
Position technique mildiou Terres Inovia 2026
L’évolution constante des races de mildiou impose une adaptation régulière des stratégies de lutte et des choix variétaux. Les observations réalisées sur le territoire national montrent que, dans la majorité des cas analysés d’attaques de mildiou sur variétés de type RM9, l’isolat en cause correspond à la race 714Pl8. C’est pourquoi il est aujourd’hui recommandé de privilégier les variétés dites RM8/9#, résistantes à cet isolat 714Pl8, dans le cas d’attaque précédente sur variété RM9.
Il convient toutefois de rappeler que les populations de Plasmopara halstedii sont en constante évolution. Aucune stratégie de lutte ne peut être considérée comme totalement durable ou absolue. Les recommandations doivent être régulièrement réévaluées en fonction des observations de terrain.
Même dans le cas de l’utilisation d’une variété résistante et d’un traitement de semence, le risque mildiou existe toujours. N’oublions jamais deux choses :
- le traitement de semences peut être lessivé en cas de grosses pluies
- et le mildiou possède une capacité d’adaptation extraordinaire face aux molécules fongicides et aux gènes de résistance des variétés.
Ces moyens de lutte doivent donc être bien utilisés afin de les faire durer :
- utiliser les bonnes pratiques agronomiques
- varier les profils RM des variétés
- utiliser raisonnablement le traitement de semence
Pour plus d’informations sur la fréquence et l’intensité du mildiou en France, retrouvez notre note commune mildiou publiée chaque fin d’année sur le site de Terres Inovia.
En savoir plus sur le mildiou du tournesol

Nos autres articles
IRRIsoja
An irrigation control tool using Watermark probes
IRRIsoja answers three key questions when irrigating soybeans:
- When to start the first round of watering?
- When to resume irrigation after a significant rainfall?
- When to stop irrigating the plot?
It is the most suitable tool for controlling soybean irrigation as closely as possible to needs, making the most of all available soil water reserves. In fact, it takes into account the type of soil in the plot, changes in soil moisture thanks to tensiometric probes, and adapts to the constraints of each farmer (duration of water turn).
IRRIsoja is specifically designed for farmers and irrigation advisors following a network of plots.
It can be downloaded free of charge by clicking on "Access the tool" above (Excel file / 1.9 MB).
Instructions for use
- IRRIsoja user guide and instructions for setting up the system (tensiometer station and tension measurement)

Camelina nutrition
Camelina requires very little fertilizer. Its powerful taproot system enables it to extract the nutrients it needs for growth from deep within the soil. Fertilization management differs according to how camelina is grown.
Camelina requires very little fertilizer. Its powerful taproot system enables it to extract the nutrients it needs for growth from deep within the soil. Fertilization management differs according to how camelina is grown
Fertilization management for camelina as a main crop
Nitrogen nutrition
Nitrogen dose trials have been carried out. Camelina yield increases with nitrogen fertilization, until it reaches a plateau (see graph below - source: Malhi et al., 2013, Canada). This yield increase is explained by improvements in several components: the number of plants per square meter, the number of branches, the number of siliques per plant, as well as the number of seeds per silique. On the other hand, thousand kernel weight (MGW) does not seem to be affected (source: Agegnehu et al.1996, USA).
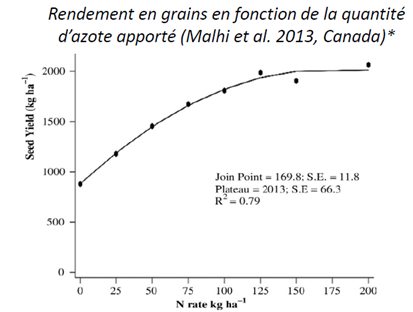
The optimum dose of nitrogen to be applied is between 80 and 100 units per hectare, depending on residues, corresponding to the economic optimum. For spring camelina, nitrogen can be applied in a single application just after sowing. However, it is possible to split the application according to the following recommendations: 30% of the dose at sowing, then the remainder at the rosette stage. For winter camelina, the application should be made when vegetation resumes before bolting.

In addition, the use of a sulfur fertilizer is recommended to ensure an application of 12 to 24 units of sulfur per hectare (source: Camelina Company).
Beware of excess nitrogen, which makes the crop more susceptible to disease, particularly albugo, and can accentuate the risk of lodging.
As nitrogen fertilization increases, so does the nitrogen content of the plant and the protein concentration of the seed. On the other hand, oil content and nitrogen use efficiency decrease (source: Malhi et al., 2013, Canada).
Concerning fatty acid composition, oleic and linoleic acid percentages increase with nitrogen dose, while linolenic acid percentage decreases. The concentration of iron (Fe) and zinc (Zn) in the seeds also decreases (source: Magdalena Czarnik et al., 2027, University of Rzeszów, Poland).
Phosphorus and potash
Camelina has moderate phosphorus and potassium requirements. Inputs should be rationed throughout the rotation, based on soil analysis results. In a well-supplied soil, we recommend applying 40 units per hectare of phosphorus and 40 units per hectare of potash. These fertilizations can be carried out at any time during the intercropping period preceding camelina planting, or directly at sowing time.
Fertilization management for camelina in summer intercropping
Camelina is a cruciferous plant. It needs nitrogen from the start of its cycle to express its full potential right up to harvest.
Managing nitrogen fertilization depends on the previous crop. In the case of cereals, 40 units of nitrogen per hectare must be applied at sowing. It is strongly recommended to apply this fertilizer locally. No additional nitrogen should be applied during vegetation. Excessive nitrogen applications could lengthen the vegetative phase of camelina, delaying maturity.
Where peas are grown before camelina, the nitrogen residue is generally sufficient to ensure good camelina development. Therefore, nitrogen is not essential. However, an optional fertilization of 10 units of nitrogen per hectare at sowing can be considered.
No background fertilization is required.

Camelina editions
Our other articles
Tour de plaine tournesol
With Tour de Plaine, Terres Inovia accompanies you to each sunflower plot to establish a health diagnosis and give you the right advice for your next sunflower crop.
This connected application also works in the absence of a telephone network.
Your health check in 5 steps:
- I locate my plot
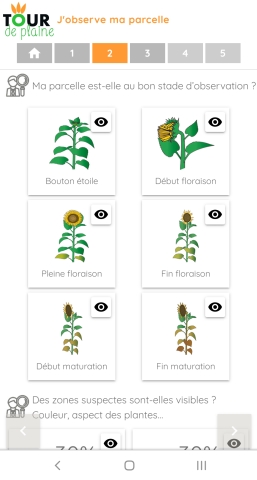
- I observe my plot
- I observe plants
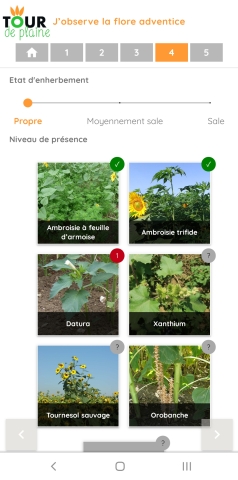
- I observe weed flora
- Terres Inovia's assessment and advice

The agronomic benefits of camelina
Camelina (Camelina sativa) is a cruciferous plant (Brassicaceae) native to Europe and Southwest Asia. It has historically been cultivated in Europe, notably in France, where the first traces date back to the Bronze Age, for the production of vegetable oil and fodder.
Camelina (Camelina sativa) is a cruciferous plant (Brassicaceae) native to Europe and Southwest Asia. It has historically been cultivated in Europe, notably in France, where the first traces date back to the Bronze Age, for the production of vegetable oil and fodder.
It was widely cultivated until the early 20th century, producing an oil used in soaps and paints, before gradually disappearing in the face of competition from more productive oilseed crops such as rapeseed. At the time, the solid residues obtained after oil extraction were used as a feed supplement for livestock or as fertilizer; the stalks were used to make brooms.
Today, it is making a comeback on the European agricultural scene, and is attracting interest from a wide range of players, both farmers and manufacturers, thanks to its agronomic advantages and the new outlets it opens up.
Good adaptation to soil and climate conditions
Camelina has one major advantage: it adapts to a wide range of soil and climate conditions, and is particularly well suited to low-potential soils. It is often presented as a hardy crop, thanks to its low input requirements and resistance to drought and high temperatures. It is also fairly tolerant of pests and resistant to lodging. Camelina requires little fertilizer or pesticide, so its introduction into cropping systems has both economic and environmental benefits.
No special equipment required, but some adjustments are necessary
What's more, it doesn't require any special equipment, making it easy to introduce to farms. Nevertheless, due to its small seed size (PMG ≈ 1-1.5g), the planting and harvesting phases require adjustments and special attention.
A short-cycle crop
An interesting feature of camelina is the length of its cycle, which varies according to variety and sowing period, from 90 to 250 days (1700 to 1900 degrees day at base 0°C, depending on variety). Camelina can therefore be grown as a main crop, in association with lentils, for example, or as a catch crop for short-cycle varieties (link to page on how to insert camelina into the SoC).
An asset for organic farming
Its low input requirements, combined with its strong competitive power - provided it emerges regularly and evenly - mean that it has a place in organic farming rotations (link to organic farming page). Some farmers even report that it has an "allelopathic" effect, i.e. that it can naturally inhibit the growth of other undesirable plants around it. To our knowledge, this has not yet been demonstrated in the field.
Conclusion
All these advantages make it a crop that can be easily integrated into a variety of cropping systems in France and around the world, in both organic and conventional farming, as a main crop or as a catch crop.